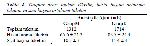|
 |
| [ Ana Sayfa | Editörler | Danışma Kurulu | Dergi Hakkında | İçindekiler | Arşiv | Yayın Arama | Yazarlara Bilgi | E-Posta ] | |
| Fırat Tıp Dergisi | |||||||||
| 2022, Cilt 27, Sayı 4, Sayfa(lar) 257-261 | |||||||||
| [ Özet ] [ PDF ] [ Benzer Makaleler ] [ Yazara E-Posta ] [ Editöre E-Posta ] | |||||||||
| Hepatektomi Ameliyatlarında Minimal Akım Anestezisi Uygulaması | |||||||||
| Yusuf Ziya ÇOLAK, Duygu DEMİRÖZ | |||||||||
| İnönü Üniversitesi Tıp Fakültesi, Anesteziyoloji ve Reanimasyon Anabilim Dalı, Malatya, Türkiye | |||||||||
| Anahtar Kelimeler: Düşük Akım Anestezisi, Minimal Akım Anestezisi, Anestezik Ajan Tüketimi, Low-Flow Anesthesia, Minimal-Flow Anesthesia, Consumption | |||||||||
| Özet | |||||||||
Amaç: Düşük akım anestezisi (DAA) %75'e varan anestezik ajan (AA) tasarrufu sağlar ve solunan anestezik gazın dinamiklerini iyileştirir, mukosilier klirensi arttırır, vücut ısısını korur ve su kaybını azaltır. DAA son yıllarda anestezi uzmanları için yüksek taze gaz akımını (TGA) önlemek için tavsiye edilmiş olsa da, DAA ve minimal akım anestezisi (MAA) kullanımı çeşitli nedenlerden ötürü sınırlıdır. Bu çalışmanın temel amacı, DAA ve MAA uygulamasının güvenli olup olmadığını araştırmaktır. İkinci amaç, bu yöntemler kullanıldığında tüketilen AA miktarını belirlemektir. Gereç ve Yöntem: Prospektif, gözlemsel olarak iki grupta çalışmaya 40 hepatektomi olgusu dahil edildi. Bir ameliyat odası sadece bu çalışma için tahsis edildi. Oksijen ihtiyacı göz önünde bulundurularak (yaklaşık 3-3.5 mL/kg/dk) 20 olgu için 300 mL/dk (grupM); 20 olgu için 600 mL/dk TGA (grupD) uygulandı. Desflurane (Suprane©) inhalasyon anestezik ajanı olarak kullanıldı ve remifentanil infüzyonu ile analjezi elde edildi. Hastaların demografik, solunum, hemodinamik, doku perfüzyon parametreleri (SpO2 ve NIRS) ve AA tüketim verileri toplanarak karşılaştırıldı. Bulgular: Gruplar arasında demografik veriler, ameliyat süresi, hemodinamik, solunum ve doku perfüzyon parametreleri açısından anlamlı bir fark saptanmamıştır. Bu parametreler tüm hastalarda her ölçüm aralığında normal sınırlar içindeydi. %40 FiO2 elde etmek için GrupD vakalarında flowmetreden ortalama %61 O2 (min=%56, maks=%65), GrupM vakalarında flowmetreden ortalama %89 O2 (min %79, maks. %100) kullanılmıştır (p <0.001). Saatlik AA tüketimi GrupMde (10.50 ± 3 mL/sa) GrupDye göre yaklaşık %34 daha düşüktü (14.10 ± 4 mL/sa). Sonuç: Hepatektomilerde güvenlik sınırlarından sapmadan 300 mL/dk TGA hızında MAA uyguladık ve AA maliyetlerini 600 mL/dk DAA uygulamasına göre yaklaşık %34 azalttık. |
|||||||||
| Giriş | |||||||||
Anestezik ilaç maliyetlerini ciddi oranda belirleyen anestezik ajanların (AA) önemli bir kısmı hasta tarafından metabolize edilmeden atık gaz sistemi üzerinden atmosfere salınır. Öte yandan, atık gaz miktarı, taze gaz akım miktarı (TGA) ile doğru orantılıdır ve TGA artışına paralel olarak artmaktadır 1. Tüm inhaler AAların atmosfer üzerinde sera gazı etkisi vardır ve bu etki desfluranda en yüksektir. Amerika Birleşik Devletleri Çevre Koruma Ajansı'nın verilerine göre, desfluranın 100 yıllık küresel ısınma potansiyeli (GWP100) 2540 gibi yüksek bir değerdir (GWP100: Farklı gazların küresel ısınma etkilerinin karşılaştırılmasına izin vermek için geliştirilmiştir. 1 ton gaz emisyonlarının belirli bir süre boyunca ne kadar enerji emeceğinin bir ölçüsüdür). Desfluranın atmosferik ömrü 14 yıldır. 2014 yılında inhaler AAın toplam yıllık küresel emisyonu, İsviçre'deki binek otomobillerin üçte birinin CO2 emisyonlarına eşdeğer olarak hesaplanmıştır ve yaklaşık %80'i desflurandan kaynaklanmaktadır 2. Bu nedenle, yüksek TGAdan kaçınmak için son yıllarda anestezi uzmanlarına düşük akım anestezisi (DAA) önerilmektedir 3. İnhalasyonel anestezi sırasında DAA (0.5-1 L/dk), solunan anestezik ajanın dinamiklerini iyileştirir, mukosilier klirensi arttırır, vücut ısısını korur ve su kaybını azaltır. Ayrıca, 2019 Dünya Tıbbi Eğilimler Raporu'na göre, küresel tıbbi enflasyon eğilimi ekonomik enflasyonunun yaklaşık üç katı kadardır (4). DAA %75'e varan ekonomik tasarruf sağlar 5. Bununla birlikte, DAA ile ilişkili riskler olarak; hipoksi, hiperkapni, yetersiz anestezi derinliği ve potansiyel olarak toksik gazların birikmesi sayılabilir. DAA, solunum gazı konsantrasyonlarını izlemek için ekipmanlarla donatılmış modern anestezi makineleri kullanılarak, riski artmadan hemen hemen tüm hastalarda kullanılabilir 6. Sonuç olarak, DAA hastalar için güvenli ve yararlıdır. Aynı zamanda ekonomik ve çevre dostudur. Benzer yorumlar minimal akım anestezisi (MAA) için de düşünülebilir (MAA=0.250.5 L/dk). Ancak hipoksi ve yüzeysel anestezi gibi kaygılar nedeniyle kullanımları yaygın değildir. Bu çalışmanın temel amacı, DAA ve MAA uygulamasının güvenli olup olmadığını araştırmaktır. İkinci amaç, bu yöntemler kullanıldığında tüketilen AA miktarını belirlemektir. |
|||||||||
| Materyal ve Metot | |||||||||
Çalışmamızı planlarken, standart bir hasta popülasyonu elde etmek için genellikle benzer vücut ağırlıklarına sahip Amerikan Anesteziyologlar Derneği fiziksel durum skoru (ASA) 1- 2 olan hepatektomi vakalarını seçtik. Prospektif, gözlemsel çalışmamız için kurumsal inceleme kurulundan etik onay alındıktan (İnönü Üniversitesi Tıp Fakültesi Klinik Araştırmalar Etik Kurulu2017/50) sonra, İnönü Üniversitesi Tıp Merkezinde, hepatektomi planlanan 18-65 yaş arası, ASA 1-2 40 hasta onamları alınarak çalışmaya dahil edildi. Diyabet hastaları, kardiyovasküler ve pulmoner hastalığı olanlar, vücut kitle indeksi <20 veya >30 olanlar, çalışmaya katılmak istemeyenler ve acil vakalar çalışma dışı bırakıldı. Operasyon öncesi anestezi cihazı (Maquet Flow-i40, Solna, Sweden) tam kontrol testinden geçirildi. Hastalara premedikasyon uygulanmadı. Hastaların yaş, boy, vücut ağırlığı (VA) ve cinsiyetleri kaydedildi. Hastaların elektrokardiyografisi (EKG), kalp atış hızı (atım/dk), sistolik arteriyel basıncı (SAB, mmHg), diyastolik arteriyel basınç (DAB, mmHg), ortalama arteriyel basınç (MAB, mmHg), periferik oksijen saturasyonu (SpO2, %) ve sıcaklık (°C) monitorize edildi. Pleth variable indeks (PVI) (intravasküler hacim durumunu değerlendirmek için), noninvaziv periferik hemoglobin (SpHb-g/dL), Perfüzyon indeksi (PI), Oksijen rezerv indeksi (ORI) monitorize edildi; Patient state indek (PSI) ve sağ ve sol spektral frekanslar (SEFL-SEFR) anestezi derinliği takibi için monitorize edildi (Root; Masimo, Irvine, CA, USA). Ayrıca serebral spektroskopi (NIRS) yöntemi ile sağ ve sol frontal bölgelerden bölgesel serebral oksimetre (rSO2L-rSO2R) ölçümü yapıldı ve bazal değerler kaydedildi (INVOS 5100C; Medtronic, MN, USA). Operasyon boyunca, doku perfüzyon parametreleri, SpO2 (%>95) ve NIRS (bazal seviyenin ±% 20'si), hastaların güvenlik aralığında olduğunu belirlemek ve hipoksiden kaçınmak için kullanıldı. Preoksijenasyon sonrası thiopental 5-8 mg/kg, fentanyl 12 mcg/kg, lidocain 1 mg/kg, vecuronium 0.1 mg/kg ile anestezi indüksiyonu yapıldı ve yeterli anestezi derinliğine ulaşıldığında uygun büyüklükte bir endotrakeal tüp takıldı. Tüm olgularda invaziv arter takibi yapıldı. Oksijen gereksinimi (≈3-3.5 mL/kg/dk) göz önüne alınarak, 20 olgu için 300 mL/dk (Minimal akım, GrupM), 20 olgu için 600 mL/dk (Düşük akım, GrupD) TGA uygulandı. Gruplar kapalı zarf yöntemiyle belirlendi. Hedenstierna araştırmasında, intraoperatif süreçte akciğerler açık tutulursa %30-40 oranında bir oksijen konsantrasyonunun (FiO2=0.3-0.4) yeterli olduğunu belirtmiştir 7. Bu nedenle tüm hastalarda hedef değerler FiO2=0.4, PSI:25-50, gruba göre bir TGA ve bu hedeflere ulaşmak için otomatik gaz kontrol modu (AGC) uygulandı. Desflurane (Suprane©) inhalasyon ajanı olarak kullanıldı, 0.5-1 mcg/kg remifentanil infüzyonu ile analjezi yönetimi sağlandı ve hastaların hiçbirinde N2O kullanılmadı. etCO2 miktarı ≥3 mmHg olduğunda CO2 absorbanı değiştirildi. Ameliyat sırasında KAH, SAB, DAB, MAB, SpO2, vücut sıcaklığı, PVI, SpHb, PI, ORI, rSO2L, rSO2R, PSI, SEFL ve SEFR değerleri bazal, anestezi indüksiyonu, entübasyon sonrası, entübasyon sonrası 10 dakika ve entübasyon sonrası 1., 2., 3., 4., 5. ve 6. saat zaman aralıklarında kaydedildi. FiO2=0.4 hedefine ulaşmak için gerekli olan O2/medikal hava oranı her on dakikada bir flowmetreden kaydedildi. Ameliyatlar sonunda toplam ameliyat süreleri ve tüketilen anestezik gaz miktarları her hasta için ayrı ayrı (anestezi cihazından) kaydedildi.
İstatistiksel Analiz |
|||||||||
| Bulgular | |||||||||
Çalışmaya 47 vaka alındı. Oksijenasyonu etkileyebileceğinden ötürü, introperatif kan transfüzyonu, inotropik veya vazokonsriktif ajan kullanımı ve hipotansiyon görülen 7 hasta çalışmadan çıkarıldı. 40 vakanın verileri analiz edildi. Gruplar arasında yaş, cinsiyet ve VA açısından anlamlı bir fark saptanmadı (Tablo 1).
Hemodinamik parametreler analiz edilen tüm vakalarda her zaman normal sınırlar içindeydi ve gruplar arası anlamlı farklılık yoktu (p =0.584). Doku oksijenasyonunun göstergesi olan SPO2 ve rSO2L, rSO2R değerleri tüm ölçüm zamanlarında güvenlik sınırlarının altına düşmedi ve gruplar arasında benzerdi (Tablo 2, 3).
Ortalama ameliyat süresi her iki grupta da benzerdi (grupM=375±78 dk, grupD=365±60 dk, p =0.529). Vücut sıcaklıkları normal aralıktaydı (min=35.9-maks=37.3°C). Tüm hastalarda PSI düzeyleri 25 ile 50 arasındaydı ve iki grup arasında herhangi bir fark saptanmadı (p =0.456). FiO2=0.4e ulaşmak için gerekli maksimum O2 konsantrasyonu GrupM için ortalama %89 (min=%79-maks=%100), GrupD için %61 (min=%56maks=%65) olarak ölçüldü. Bu fark istatistiksel olarak anlamlıydı (p <0.001). GrupM'deki üç vakada, FiO2=0.4'ü korumak için operasyon sırasında kısa bir süre için flowmetreden %100 oksijene oranına ihtiyaç duyuldu. Saatlik AA tüketimi GrupD'de (14.10 ± 4 mL/sa) GrupM'e (10.50± 3 mL/sa) göre ≈ %34 daha yüksekti. Toplam tüketim GrupM'de 1312 mL olarak ölçülürken, vaka başına ortalama 65.60 ± 21.30 mL, GrupD'de toplam tüketim 1714 mL olarak ölçülürken, vaka başına ortalama 85.70 ± 24.40 mL oldu (Tablo 4).
|
|||||||||
| Tartışma | |||||||||
DAA ve MAA'de oksijenlenme ve anestezi derinliği iki ana endişedir. İnsanlar için ideal O2 seviyesi %21'dir ve kandaki ideal PaO2 yaklaşık 100 mmHg'dir. Oksijeni bir ilaç olarak göz önüne alındığımızda, birçok çalışma sadece düşük oksijen seviyelerinin riskli olmadığını, aynı zamanda yüksek seviyelerin de riskli olduğunu göstermiştir 7. Bu nedenle oksijenlenme mümkün olduğunca ideal seviyelere yakın yapılmalıdır. Bu amaç için en sık kullanılan formül Brody formülüdür (VO2=10XVA3/4), ayrıca tahmini oksijen talebi yaklaşık 3-5 mL/kg/dk olarak hesaplanabilir 8. Her iki gruptaki deneklerin ortalama ağırlığı 70 kg civarındaydı ve benzerdi. Bu vücut ağırlığına göre hesaplama yapıldığında yaklaşık bazal metabolik O2 ihtiyacı ≈250 mL/dk olarak bulunabilir (Brody formülüne göre). GrupM'de TGA, 300 mL/dk (Modifiye Baker-Simionescu sınıflamasına [MBSs] göre MAA) ve grupD'de TGA, 600 mL/dk (MBSsna göre DAA) olarak belirlenmiştir. Bu TGA miktarları yukarıda hesapladığımız gerekli O2 miktarını sağlamak (≈250 mL/dk) için teorik olarak yeterlidir. Bulgularımızda belirtildiği gibi, FiO2=0.4 oranını elde etmek için flowmetreden ayarladığımız TGA içindeki maksimum O2 konsantrasyonu GrupDde %61 (min%=56-maks=%65), GrupMde %89 (min=79% - maks=100%) idi. Bu sayılar 300 mL/dk TGA'da bile bir güvenlik aralığı olduğunu gösterdi. Ayrıca her durumda çalışmamızda takip ettiğimiz hemodinamik ve oksijenasyon parametrelerinin (SpO2, rSO2) güvenlik sınırlarını aşmaması yukarıda belirtildiği gibi sonuçlarımızı desteklemektedir. Üç vaka FiO2=0.4 oranını korumak için kısa bir süre için flowmetreden %100 O2 oranına ihtiyaç duydu, ancak bu olguların SPO2 ve NIRS değerleri aynı zaman diliminde normal aralıktaydı. Bununla birlikte, bu vakaların hesaplanan O2 ihtiyacı grup ortalamasına yakındı. Bu durumun solunum sistemi kaçaklarına bağlı olabileceğini tahmin edebiliriz. DAA uygulamalarında sistem kaçakları çok önemli bir sorundur. Anestezi makinemiz gelişmiş sensörlere ve uyarı sistemlerine sahiptir, ancak ne yazık ki sistem kaçağı testi için kabul edilebilir üst limit 150 mL/dk'dır (diğer gelişmiş modern anestezi makineleri gibi), bu kadar düşük akımlarda çalışırken 150 mL/dk civarı kaçak önemli bir sorun oluşturabilir. Mümkünse, düşük akımlarda çalışırken solunum sistemi kaçağı olmamalıdır. GrupM'de kullandığımız 300 mL/dk TGA, MBS sınıflandırmasına göre MAA'ya eşittir. GrupD'de kullandığımız 600 mL/dk TGA, MBS sınıflandırmasına göre DAA'ya eşittir. 1 L/dk TGA'nın altındaki bu iki değer arasında bile AA maliyetinde ≈ %34 fark vardı. TGA miktarları arasındaki fark azaldığında tüketim farkları da azalır, bu beklenen bir durumdur. Benzer bir çalışmamızda 9, AA tüketiminde 600 mL/dk TGA (AA tüketimi=12.40 mL/sa) ile 1200 mL/dk TGA (AA tüketimi=21.50 mL/sa) arasında ≈ %43 fark vardı. Bu çalışma, 600 mL/dk TGA ile 300 mL/dk TGA arasında yapıldı, ancak daha yüksek bir TGA ile yapılacak karşılaştırmalarda AA tüketim miktarlarındaki fark çok daha fazla olacaktır. 2021 fiyatlarına göre bir 240 mL desfluranın fiyatı 338 TL olup GrupM için saatlik AA maliyeti 14.78 TL, GrupD için saatlik AA maliyeti 19.85 TL, fark ≈5 TLdir. Bir anestezi cihazının günde 6 saat çalıştığını düşünürsek, 12 odalı bir ameliyathanede yıllık AA maliyeti tasarrufu ≈130.000 TL olacaktır. Bu farkın ekonomik açıdan önemli olduğunu düşünüyoruz. Tekrar belirtmek gerekirse bu fark DAA ve MAA arasındaki tasarruf miktarıdır. Orta ve yüksek akımlar düşünüldüğünde tasarruf miktarı çok daha fazla olacaktır. AA ile ilgili bir diğer önemli sorun atmosferik sera gazı etkileridir. Atık gaz sistemine giren gazlar ameliyathaneden atmosfere salınır ve atık gaz sistemine giren AA miktarının ana belirleyicisi TGA miktarıdır. Bu nedenle, atık anestezik gazların miktarını ve çevresel kirlenmeyi azaltmayı amaçlayan yöntemler TGA miktarına odaklanmaktadır 10. Bu çalışmada, TGAda %50'lik bir düşüş ile AA tüketiminde ≈ %34 azalma sağladık. Tek bir vakanın çevresel etkisi az olabilir, ancak bir anestezi uzmanının tüm kariyeri boyunca ürettiği atık gaz miktarı veya tüm dünyada bir günde inhalasyon anestezisi altında yapılan ameliyatlar göz önüne alındığında durumun ciddiyeti daha iyi anlaşılacaktır. Buna ek olarak, çalışan güvenliği açısından, ameliyathane ortamının atık gazla kirlenmesinin engellenmesi önemlidir. Gauger ve ark. atık gaz miktarına daha fazla maruz kalan pediatrik anestezistler ile diğer anestezi uzmanlarını karşılaştıran bir çalışma yürüttü ve pediatrik anestezistlerde spontan abortus oranlarının daha yüksek olduğunu buldu 11. Çalışmamızın bazı sınırlamaları vardır. İlk olarak, CO2 absorban maliyeti AA ile karşılaştırıldığında çok düşük olduğundan CO2 absorban maliyetini hesaplamadık. Bir diğer sınırlama da cihazlar vaka alınmadan hemen önce tam testten geçirilsede, çok az da olsa devre kaçaklarının kaçınılmaz olmasıydı (kaçak alarm üst limit ≥150 mL/dk). DAA veya MAA'de, TGA ne kadar düşükse, kaçak miktarı o kadar önemli hale gelmektedir. |
|||||||||
| Sonuç | |||||||||
Yüksek teknolojili anestezi cihazlarımız ve monitörlerimiz ile uygun vakalarda DAA/MAA kullanmak, AAların çevresel etkilerini azaltmak ve maliyetleri en aza indirmek için mantıklı bir seçenektir. Bu çalışmada, hepatektomilerde FiO2=0.4 oranına, 300 mL/dk TGA (MAA) ile güvenli bir şekilde ulaştık ve AA maliyetini 600 mL/dk TGAna (DAA) göre ≈ %34 azalttık. |
|||||||||
| Kaynaklar | |||||||||
1) Nair BG, Peterson GN, Neradilek MB et all. Reducing wastage of inhalation anesthetics using real-time decision support to notify of excessive fresh gas flow. Anesthesiology 2013; 118: 874-84.
2) Karin LZ, Shannon KB, Lana MV et all.Provider education and vaporizer labelling lead to reduced anesthetic agent purchasing with cost savings and reduced greenhouse gas emissions. Anesth Analg 2019; 128: 97-9.
3) Sherman J, Le C, Lamers V, EckelmanM. Life cycle greenhouse gas emissions of anesthetic drugs. AnesthAnalg 2012; 114:1086-90.
4) Mercer Marsh Benefits, 2019 Medical Trends Around The World Report. Marsh&McLennan Companies. https://www.mmc.com/content/dam/mmc-web/insights/publications/2019/jun/MMB_Medical_Trends_Survery_Final.pdf
5) Hönemann C, Hagemann O, Doll D. Inhalational anaesthesia with low fresh gas flow. Indian J Anesth 2013; 57: 345-50.
6) Suttner S, Boldt J. Low-flow anaesthesia does it have potential pharmacoeconomic consequences? Pharmacoeconomics 2000; 17: 585-90.
7) Hedenstierna G. Oxygen and anesthesia: what lung do we deliver to the post-operative ward? Acta Anaesthesiol Scand 2012; 56: 675-85.
8) Baker AB. Low flow and closed circuits. Anaesth Intensive Care 1994; 22: 341-2.
9) YZ Colak YZ, Toprak HI. Feasibility, safety, and economic consequences of using low flow anesthesia according to body weight. J Anesth 2020; 34: 537-42.
10) Baum JA, Aitkenhead AR. Low-flow anaesthesia. Anaesthesia 1995; 50: 37-44.
|
|||||||||
| [ Başa Dön ] [ Özet ] [ PDF ] [ Benzer Makaleler ] [ Yazara E-Posta ] [ Editöre E-Posta ] | |||||||||
| [ Ana Sayfa | Editörler | Danışma Kurulu | Dergi Hakkında | İçindekiler | Arşiv | Yayın Arama | Yazarlara Bilgi | E-Posta ] |